Le Molecole Biologiche

Le Molecole Biologiche o Biomolecole sono le molecole alla base della vita. Sono formate essenzialmente da uno scheletro in carbonio e idrogeno, lungo il quale sono presenti anche altri elementi, come ossigeno, azoto, fosforo e zolfo.
Sono tutte Macromolecole, cioè hanno alto peso molecolare. La maggior parte sono anche dei polimeri, cioè grandi molecole formate da molecole più piccole detti monomeri. Quando tutti i monomeri sono uguali prende il nome di omopolimero, quando i monomeri sono differenti prende il nome di copolimero.
I monomeri si legano fra loro sfruttando dei legami chimici, in particolare secondo una reazione chiamata polimerizzazione, più precisamente policondensazione.
Perché questa reazione avvenga i monomeri devono avere i seguenti requisiti:
- Devono essere molecole organiche con gruppi funzionali
- Almeno un monomero deve avere un gruppo ossidrile (-OH)
- I monomeri devono avere i gruppi funzionali vicini
- Dall'unione dei due monomeri si deve poter formare una molecola d'acqua (H2O)
Le Biomolecole posso riassumersi in 4 gruppi:
- Carboidrati
- Proteine
- Lipidi
- Acidi Nucleici
Carboidrati
I Carboidrati, o meglio glucidi (quando derivati dal glucosio), glicidi o più comunemente "zuccheri", costituiscono una delle 4 classi di molecole organiche essenziali per la vita di ogni organismo.
I principali atomi costituenti infatti sono: carbonio, idrogeno e ossigeno.
La corretta definizione di Glucidi, adottata dalla comunità scientifica, è: "composti organici contenenti funzioni carboniliche (aldeidiche o chetoniche) e funzioni alcoliche"
Le funzioni dei carboidrati sono differenti:
-
Ricoprono un importante ruolo energetico. Difatti, il glucosio è il principale combustibile da cui i viventi ricavano energia.
Nel mondo vegetale il glucosio è sintetizzato a partire dai processi fotosintetici, che vedremo in seguito.
I carboidrati possono produrre energia fino a 4,15 kcal/g. - Costituenti strutturali degli organismi vegetali, basti pensare alla cellulosa, o animali, molto presenti nelle cartilagini.
- Costituenti di base per le altre molecole biologiche. Gli acidi nucleici, per esempio, sono formati a partire da uno zucchero pentoso.
- Altri zuccheri sono presenti come coenzimi (attivatori degli enzimi), nelle vitamine, negli antibiotici e nella parete cellulare dei batteri.
I singoli monomeri dei carboidrati prendono il nome di monosaccaridi, i quali presentano un solo gruppo funzionale, tra cui possiamo trovare Glucosio, Fruttosio, Galattosio, Ribosio, Desossiribosio e Mannosio.
I monosaccaridi sono chiamati "aldosi" o "chetosi" a seconda della funzione carbonilica che possiedono (se sono appunto aldeidi o chetoni).
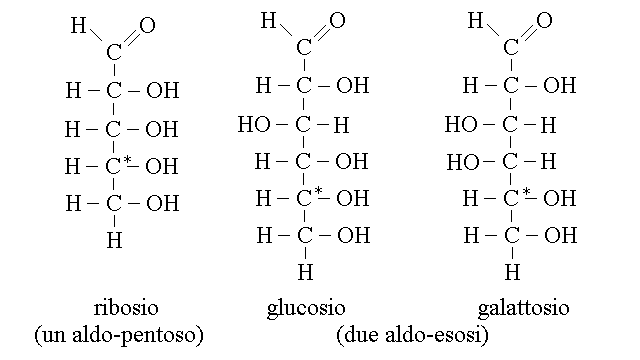
Abbiamo poi i Disaccaridi, formati dalla policondensazione di due monosaccaridi.
Abbiamo ad esempio il Saccarosio, formato da Glucosio e Fruttosio.

I Polisaccaridi invece sono carboidrati che si ottengono dall'unione per policondensazione di molti monosaccaridi, da centinaia a migliaia. I più conosciuti sono Amido,
Glicogeno e Cellulosa.
Se per idrolisi un polisaccaride da un solo tuoi di monomero allora esso prende il nome di Omopolisaccaride, se invece è costituito da monomeri diversi è chiamato
Eteropolisaccaride.
- L'Amido è un polisaccaride di riserva energetica degli organismi vegetali. Esso è costituito da due frazioni: l'amilosio e l'amilopectina. L'Amilosio, solubile in acqua, è formato da 50 a 300 monomeri di glucosio, disposti in catene lineari. L'Amilopectina presenta invece ramificazioni ed è costituita da 300 a 5000 monomeri.
- Il Glicogeno costituisce la riserva energetica degli organismi animali, nei quali viene conservato nel fegato e nel tessuto muscolare. Questa molecola presenta molte ramificazioni, ogni 8-10 unità.
- La Cellulosa, il composto più diffuso in natura, svolge invece una funzione strutturale, formando la parete delle cellule vegetali. Strutturalmente è composta da catene lineari, disposte parallelamente, unite da legami a idrogeno che rendono la molecola stabile e resistente. Gli erbivori sono gli unici organismi a possedere gli enzimi necessari per scinderla e per poterla utilizzare come riserva energetica.
Abbiamo poi Carboidrati Complessi, all'interno dei quali sono presenti altri gruppi di atomi che ne determinano le caratteristiche chimico-fisiche. Come sostituenti abbiamo: gruppi fosfato, gruppi amminici o acetilici.
Le reazioni chimiche dei carboidrati sono: Addizione Nucleofila al Carbonile (Emiacetilizzazione), la quale può avvenire all'interno di una stessa molecola provocandone la ciclizzazione, l'Acetilizzazione e l'Ossidazione.
Emiacetilizzazione:
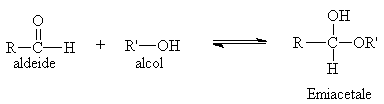
Acetilizzazione:

Ossidazione: con ossidanti blandi si ossidano solo le aldeidi, con ossidanti forti riusciamo ad ossidare sia aldeidi che chetoni (condizioni drastiche).

Proteine
Le Proteine sono la seconda classe di molecole biologiche. Sono formate a partire da polimeri, molecole ad alto peso, composte a partire dall'unione per policondensazione di molti monomeri chiamati amminoacidi. Questi legami possono essere rotti da variazioni di pH, sbalzi di temperatura o trattamenti chimici effettuati male.
Si parla di Peptidi quando sono uniti solo pochi amminoacidi, di Polipeptidi quando si possono conteggiare fino a 50 diversi amminoacidi e di Proteine vere e proprie quando la catena polipeptidica ottiene una conformazione spaziale (tridimensionale).
Un amminoacido è formato da: un gruppo carbossilico, un gruppo amminico e un gruppo "R" che caratterizza un amminoacido specifico.
R
|
H3N-C-COOH
|
H
Gli amminoacidi si possono classificare in: Polari o Apolari e Essenziali e Non essenziali.
Gli amminoacidi polari hanno gruppo R polare affine all'acqua (Serina), mentre quelli apolari hanno gruppo R idrofobo (Glicina, Alanina o Cisteina).
Gli amminoacidi essenziali sono gli amminoacidi che il nostro corpo non è in grado di produrre. Sono 8 ed è necessario introdurli attraverso l'alimentazione.
Gli amminoacidi non essenziali sono invece prodotti dal nostro corpo, perciò non è necessario introdurli, sono 20.
Quando due o più amminoacidi si legano tra di loro il legame prende il nome di legame peptidico o legame ammidico.

Le proteine possono avere fino a 4 livelli di organizzazione strutturale.
Il primo livello è detto Struttura Primaria, ed è definito dalla sequenza degli amminoacidi legati tra di loro.
Il secondo livello, la Struttura Secondaria, è dato da un ripiegamento nello spazio del primo livello. Solitamente questo avviene secondo due forme: o a foglietti pieghettati oppure ad alfaelica (visibile nell'immagine sottostante).
Il terzo livello, Struttura Terziaria, corrisponde ad un secondo ripiegamento della catena, che però mantiene entrambe le strutture precedenti. Dopo questo passaggio la molecola può avere forma globulare (tipica delle proteine di trasporto) oppure a cordone (tipica delle proteine di struttura).
Il quarto livello, Struttura Quaternaria, è il più complesso e non è presente in tutte le proteine (a differenza dei primi tre che sono sempre presenti). Esso è costituito dall'unione di più catene di amminoacidi, ciascuna con livelli fino al terzo, nei quali possono andare ad inserirsi anche atomi aggiuntivi.

Anche le proteine ricoprono funzioni differenti:
- Hanno funzione strutturale, poiché costituiscono per il 20% le membrane cellulari.
- Proteine come l'Actina e la Miosina ci consentono il movimento perché hanno un ruolo nella contrazione muscolare.
- Hanno ruolo difensivo, costituiscono gli anticorpi.
- Hanno ruolo di regolazione dei processi vitali, dal momento che molti ormoni sono proteici.
- Molecole essenziali, come Emoglobina e Cheratina, sono proteine.
- Molti Enzimi sono di natura proteica.
Prendiamo due esempi: emoglobina e lisozima.
L'emoglobina è una proteina complessa, che possiede fino al quarto livello strutturale. E' formata dall'unione di 4 catene polipeptidiche, ciascuna di 150 amminoacidi, che hanno una precisa struttura primaria. La struttura secondaria delle quattro catene presenta forma ad alfaelica e struttura terziaria di forma globulare. Anche l'ultimo livello mantiene forma globulare, dove si aggiunge un gruppo aggiuntivo di atomi chiamato gruppo eme, contenente ferro.
La funzione principale dell'emoglobina è il trasporto dell'ossigeno che si legherà al gruppo eme e verrà diffuso all'interno del corpo.
Il Lisozima è una proteina formata da 3 livelli strutturali misti, che svolge funzione enzimatica.
E' contenuto all'interno della saliva e consiste in una delle prime difese dell'organismo dall'attacco di sostante e organismi estranei.
Lipidi
NB: Definiamo ora i caratteri principali di lipidi. Per informazioni più dettagliate rispetto le varie classi appartenenti ai lipidi sono disponibili gli approfondimenti sottostanti.
I lipidi, conosciuti anche come grassi, sono la terza classe di molecole biologiche.
A differenza degli altri gruppi di molecole, i lipidi non sono in grado di polimerizzare, quindi
mantengono peso molecolare più bassi.
Sono largamente diffusi in natura e sono presenti in tutte le cellule, animali e vegetali.
Ai lipidi appartengono categorie di molecole anche molto diverse tra di loro, le quali hanno tutte
proprietà specifiche, anche molto diverse tra di loro.
Strutturalmente sono costituiti da lunghe catene formate da atomi di carbonio e idrogeno.
Sono presenti diverse tipologie di classificazione dei lipidi:
-
In base alla capacità di solubilizzarsi o meno in acqua. Se sono solubili in acqua
prendono il nome di idrofili, se al contrario NON sono insolubili vengono definiti idrofobi (sono solubili in solventi organici come l’ acetone, alcoli e idrocarburi).
- Divisi in otto classi, classificazione dell’International Lipid Classification and Nomenclature Committee, in base alla presenza di due unità costitutive fondamentali:
|
unità isopreniche (-C5H8-). |
|
unità chetoaciliche (-CH2-CO-) |
-
Classificati in Saponificabili (Gliceridi, Fosfolipidi, Cere) e non Saponificabili (Terpeni, Steroidi, Vitamine liposolubili),cioè se sono
solubili in fase acquosa dopo un trattamento con alcani.
- Divisi in Acidi Grassi Saturi, se la catena carboniosa contiene solo legami semplici C-C, e Insaturi se sono presenti doppi legami che piegano la molecola formando dei "gomiti". Possono assumere conformazione Cis o Tras a seconda della geometria della molecola.

-
Classificati in base agli atomi che compongono la molecola.
I Lipidi Semplici Sono costituiti da carbonio, idrogeno e ossigeno.
I lipidi Complessi sono costituiti da carbonio, idrogeno, ossigeno e fosforo o azoto e sono sintetizzati con una reazione di esterificazione tra acidi grassi e alcoli (sono costituiti da esteri del glicerolo).
I Lipidi Derivati, dalla trasformazione di lipidi semplici o composti.
I lipidi hanno una densità minore rispetto a quella dell'acqua, per questo possiamo vederli raggruppati in goccioline sulla superficie.
In base alle interazioni che hanno con l'acqua, i lipidi sono raggruppati in 3 classi:
I lipidi non polari (idrocarburi alifatici a lunga catena, idrocarburi aromatici voluminosi, esteri ed eteri, in cui entrambi i componenti sono
lipidi idrofobi voluminosi) sono completamente insolubili in acqua e non si allineano.
I lipidi polari di classe I sono molecole che presentano un'estremità debolmente polare. I lipidi polari di II classe presentano
un'estremità idrofobica e una idrofila (con le teste polari immerse nella soluzione acquosa e le code idrofobe immerse nella fase gassosa soprastante).I lipidi polari di III
classe hanno una molecola fortemente polare, rispetto alla regione idrofobica, e sono insolubili in olio.
Le proprietà chimiche invece dipendono dalle varie classi di lipidi.
Le funzioni che i Lipidi ricoprono sono principalmente 4:
-
Riserva Energetica
I lipidi rappresentano un'importante riserva energetica per animali e piante, in quanto sono in grado di liberare una grande quantità di calorie per unità di massa ( circa il doppio rispetto a zuccheri e proteine, circa 9,46 kcal/g verso 4,15 kcal/g, dal momento che sono più facilmente ossidabili rispetto ai carboidrati perché hanno meno atomi di ossigeno, dovuti ai gruppi alcolici).
-
Isolamento dal Freddo
Il loro deposito di grassi vicino a organi importanti (come cuore, fegato, milza, reni, cervello e midollo spinale) rappresenta un importante protezione meccanica e il deposito nel sottocute svolge un ruolo isolante contro le basse temperature, dal momento che i tessuti grassi non sono irrorati da molti vasi, quindi sono in grado di non disperdere il calore accumulato.
-
Formazione delle Membrane Cellulari
I fosfolipidi hanno una funzione strutturale insostituibile nella formazione delle membrane biologiche: grazie alla loro idrofobicità, consentono di tenere separati compartimenti acquosi di differente composizione, condizione essenziale per permettere la vita.
-
Funzione Ormonale e altre Funzioni all’interno dell’Organismo
Alcuni lipidi agiscono da messaggeri intracellulari. Diversi ormoni e mediatori chimici (extracellulari) sono di natura lipidica. Inoltre, alcune vitamine, gli ormoni corticosurrenali e gli ormoni sessuali (estrogeni, progesterone e androgeni) sono steroidi e alcune vitamine appartengono alla classe dei terpeni, mentre le prostaglandine e i leucotrieni derivano da acidi grassi polinsaturi, tutti classificati come Lipidi.
Approfondimenti sui lipidi a cura della classe 4S (2013/2014) dell'Istituto Itas Selmi (MO)
Per approfondimenti ulteriori visitate anche Lipids Webquest
Ringraziamo Arianna Bisini e Nica Alexandra per questo approfondimento.
Acidi Nucleici
Gli Acidi Nucleici sono la quarta classe di molecole biologiche fondamentali per la vita di ogni organismo.
Sono le molecole più complesse, infatti sono state le ultime ad essere scoperte, isolati e scoperti da F. Miescher nel 1870 e meglio studiati da Whatson e Crick nel 1953.
Sono polimeri, i cui monomeri prendono il nome di nucleotidi.
Ogni nucleotide è costituito da 3 molecole: uno zucchero pentoso, un gruppo fosfato e una base azotata.
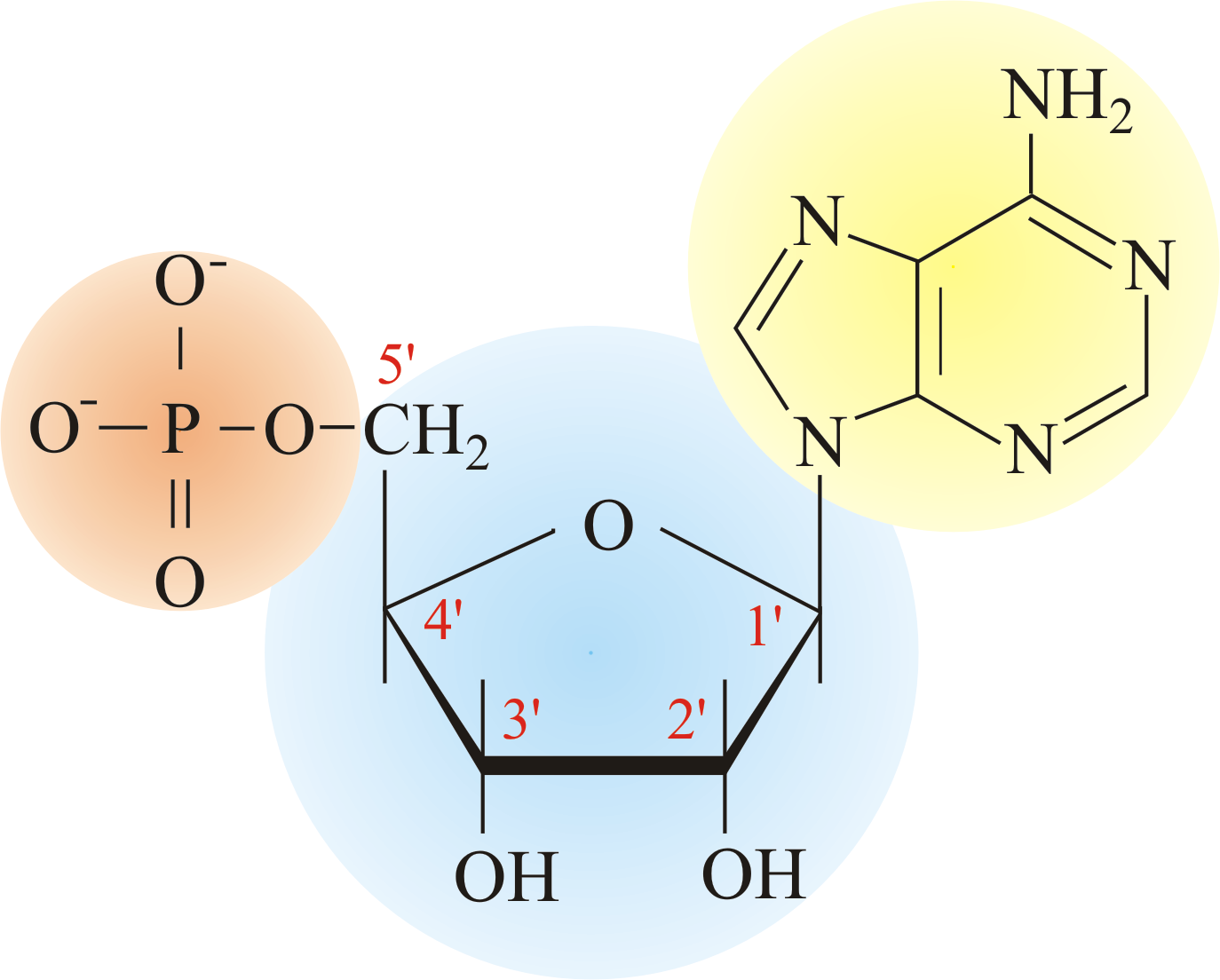
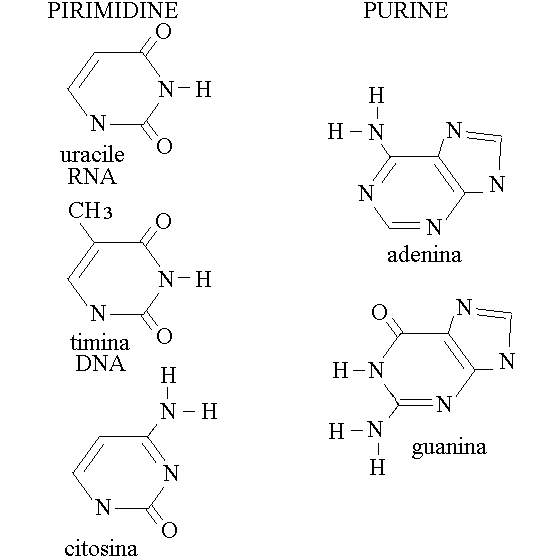
Le basi azotate possono essere di due tipi, pirimidiniche e puriniche.
Le basi Pirimidiniche sono Timina, Citosina e Uracile, sono costituite da un solo anello esagonale sul quale due carboni sono sostituiti da due
idrogeni.
Le basi Puriniche sono Guanina e Adenina e sono formate da due anelli condensati.
I due acidi nucleici sono il DNA, che si trova nel nucleo delle cellule Eucarioti e nel citoplasma di quelle Procarioti, e
l'RNA, presente nel citoplasma di entrambe.
Il DNA (o acido desossiribonucleico) è formato dallo zucchero pentoso Desossiribosio e ha come
basi Adenina, Citosina, Guanina e Timina. In addizione alla normale catena di amminoacidi presenta altri due livelli strutturali, come le proteine. Il DNA possiede un livello
strutturale secondario, dove abbiamo due catene appaiate e complementari che si avvolgono ad elica, i quali procedono in direzioni opposte. Tra le basi azotate si formano legami a
idrogeno e abbiamo un appaiamento chimico-spaziale tra le basi azotate.
Per mantenere sempre i due filamenti alla stessa distanza è infatti necessario che si accoppino una base purinica e una pirimidinica. Inoltre Adenina e Timina hanno
stesso numero di siti attivi, stesso discorso per Citosina e Guanina: abbiamo quindi un appaiamento specifico e obbligatorio A-T C-G.
Per questo possiamo anche dire che:
- La composizione percentuale di basi è tipica di ogni organismo ed è uguale in ogni sua cellula.
- La composizione percentuale di Adenina è uguale a quella di Timina. La stessa cosa vale per Citosina e Guanina.
- La composizione percentuale di basi puriniche è uguale a quella delle basi pirimidiniche.
Il DNA viene poi avvolto attorno a proteine chiamati istoni, conferendogli una struttura spaziale "terziaria" detta cromatina, la quale può organizzarsi a sua volta per formare i cromosomi.
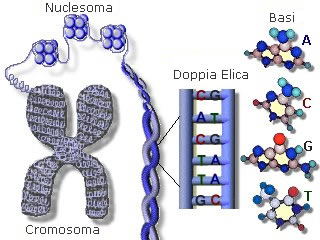
La funzione del DNA è quella di contenere tutte le informazioni genetiche che caratterizzano un organismo, sia dal punto di vista strutturale che
funzionale.
Questa molecola consente anche di trasferire le informazioni genetiche da una cellula madre ad una cellula figlia ed è quella che regola tutti i processi della
cellula.
L' RNA (o acido ribonucleico) è formato dallo zucchero pentoso Ribosio e ha come
basi Adenina, Citosina, Guanina e Uracile, le quali si appaiano esattamente come per il DNA, tranne per il fatto che l'Uracile sostituisce la
Timina.
Le molecole di RNA sono costituite da singole catene polipeptidiche, che presentano una sequenza di basi complementare a quella del DNA (se per esempio nel DNA
abbiamo ACG nell'RNA avremo UGC). Ogni filamento di RNA può presentarsi sotto tre forme e svolge le sue funzioni all'interno del citoplasma cellulare.
L'mRNA o RNA messaggero è un semplice filamento lineare, che si occupa di trasferire le informazioni genetiche dal nucleo al
citoplasma.
L'rRNA o ribosomiale è un filamento che si avvolge su sé stesso, formando un piccolo organulo cellulare. Esso partecipa alla
sintesi delle proteine.
Abbiamo poi il tRNA o transfer, filamento ripiegato ad una estremità, lungo il quale ogni tripletta di basi costituisce
un codone che codifica una amminoacido preciso, sintetizzando la struttura primaria di ogni proteina.



